Introduction
Dans cet article, nous cherchons à démontrer l’impact d’une ou plusieurs intoxications alimentaires aiguës dans la genèse de troubles fonctionnels digestifs chroniques, notamment le syndrome du côlon irritable post-infectieux (SII-PI) [1] et le SIBO (Small Intestinal Bacterial Overgrowth) [2] . Ces pathologies trouvent souvent leur origine dans un épisode infectieux apparemment banal, mais capable de laisser une empreinte durable sur la motilité intestinale et l’équilibre du microbiote.
Définition de l’intoxication alimentaire
Une intoxication alimentaire est un trouble digestif aigu résultant de la consommation d’aliments ou de boissons contaminés par des micro-organismes pathogènes (bactéries, virus, parasites) ou par leurs toxines. Elle se manifeste typiquement par des diarrhées, douleurs abdominales, nausées et/ou vomissements, survenant de manière soudaine.
Selon la littérature scientifique, les bactéries les plus fréquemment impliquées dans les intoxications alimentaires sont :
Staphylococcus aureus ou Bacillus, Clostridium perfringens, Escherichia coli pathogènes, Shigella, Salmonella enterica
Mécanismes physiopathologiques d’une intoxication alimentaire aiguë
Une intoxication alimentaire aiguë résulte de la pénétration dans l’organisme d’agents pathogènes (bactéries, virus, parasites) ou de leurs toxines. Les mécanismes en jeu sont aujourd’hui bien connus et expliquent la symptomatologie digestive brutale observée après ingestion d’un aliment contaminé.
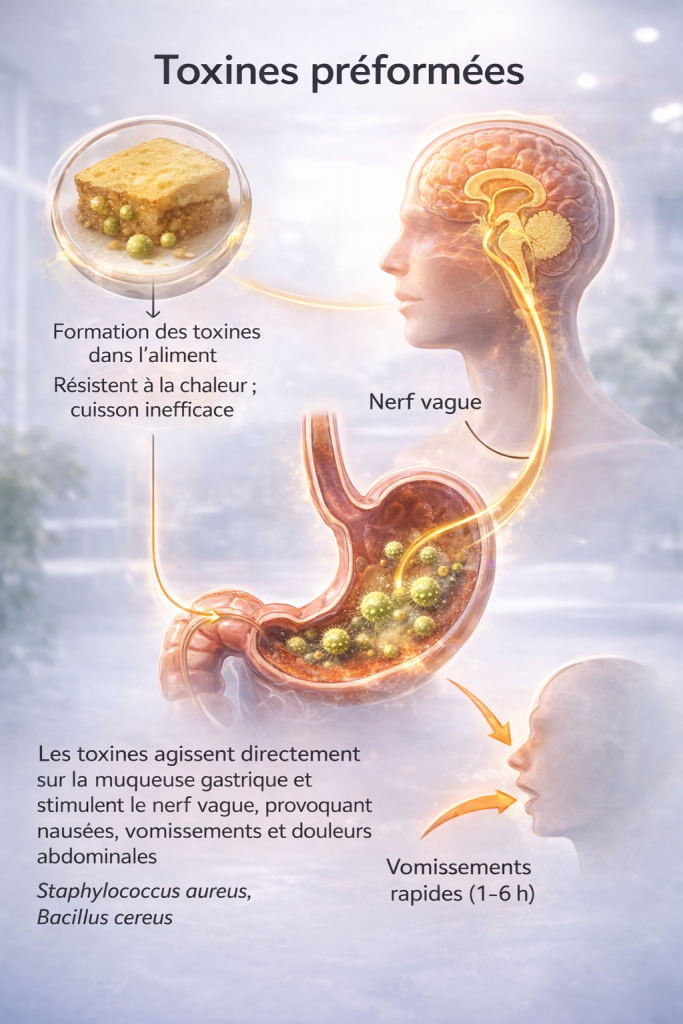
- Action directe des toxines préformées
Certaines bactéries comme Staphylococcus aureus ou Bacillus cereus produisent des entérotoxines déjà présentes dans l’aliment. Ces toxines stimulent les récepteurs vagaux et le centre du vomissement, expliquant la survenue très rapide des nausées et vomissements (1 à 6 heures après ingestion), souvent sans fièvre.
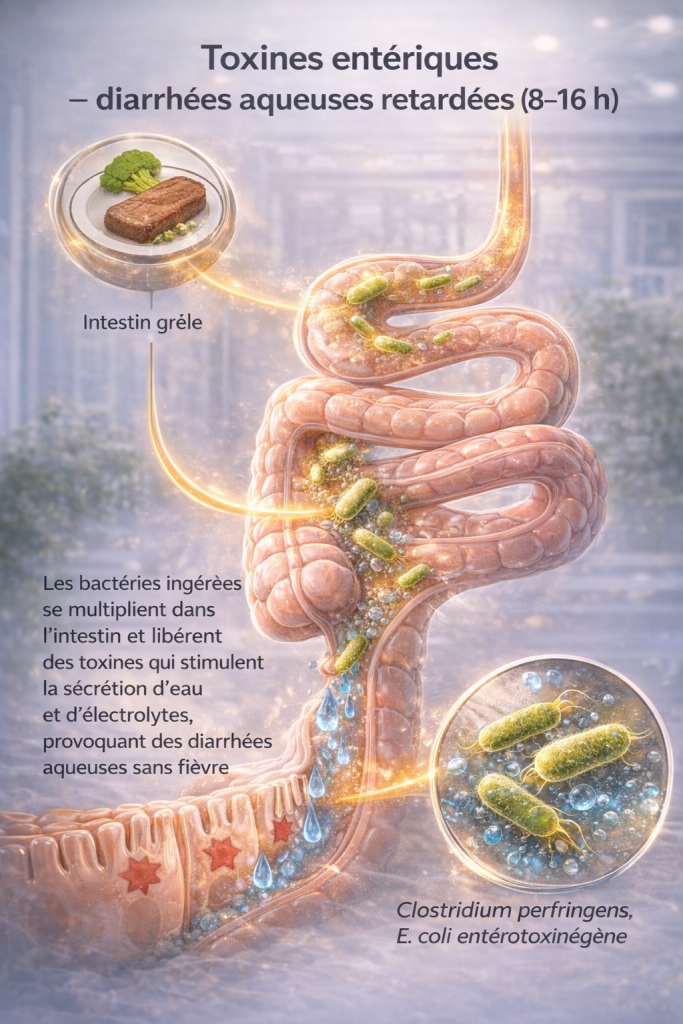
2. Colonisation intestinale et production de toxines in sit
D’autres germes, tels que Clostridium perfringens ou certaines souches d’Escherichia coli, prolifèrent dans le tube digestif après ingestion et sécrètent des toxines altérant la perméabilité des entérocytes. Il s’ensuit une fuite d’eau et d’électrolytes responsable de diarrhées aqueuses, parfois abondantes.
3. Invasion et inflammation de la muqueuse
Des bactéries entéro-invasives comme Salmonella, Shigella ou Campylobacter jejuni traversent la barrière intestinale, induisant une inflammation aiguë, la destruction des cellules épithéliales et une réponse immunitaire locale. Cette réaction s’accompagne de douleurs abdominales, de fièvre et de diarrhées sanglantes ou mucoïdes.
4. Perturbation transitoire de la motricité intestinale
L’inflammation, la douleur et les médiateurs sécrétés localement (cytokines, prostaglandines) entraînent une altération temporaire de la motricité intestinale : ralentissement, spasmes ou accélération du transit. Ces perturbations disparaissent habituellement après la résolution de l’infection, mais peuvent, dans certains cas, laisser une empreinte durable sur le fonctionnement du système nerveux entérique.
Certaines bactéries, notamment E. coli, Campylobacter, Shigella ou Salmonella, sont connues pour perturber le Complexe Moteur Migrant (CMM), un mécanisme clé de la motricité intestinale, dont la désorganisation peut contribuer à l’apparition ultérieure de troubles digestifs chroniques (SII post-infectieux, SIBO).
La motilité intestinale
La motilité intestinale correspond à l’ensemble des mouvements coordonnés du tube digestif qui permettent aux aliments, puis aux résidus alimentaires, de progresser de la bouche jusqu’à l’anus.
Ces mouvements sont indispensables au bon fonctionnement digestif : sans eux, la digestion, l’absorption des nutriments et l’élimination des déchets seraient impossibles.
La motilité fait donc partie intégrante du système digestif et joue un rôle central dans l’équilibre intestinal.
Lorsqu’elle est altérée, elle peut être à l’origine de nombreux troubles fonctionnels, notamment des ballonnements, une sensation de ventre gonflé, une digestion lente ou inconfortable.
Il est important de comprendre cette motilité, car les stratégies visant à la restaurer ou à l’optimiser permettent souvent d’améliorer significativement ces symptômes digestifs.
On distingue trois grands types de mouvements intestinaux, qui interviennent à des moments précis et remplissent des fonctions différentes.
1. La motilité postprandiale (juste après le repas)
Après un repas, l’intestin entre dans une phase appelée motilité postprandiale. Cette phase a pour objectif principal de digérer, mélanger et absorber efficacement les nutriments issus des aliments.
3 types de mouvements dominent alors : le péristaltisme, la segmentation et le CMM.
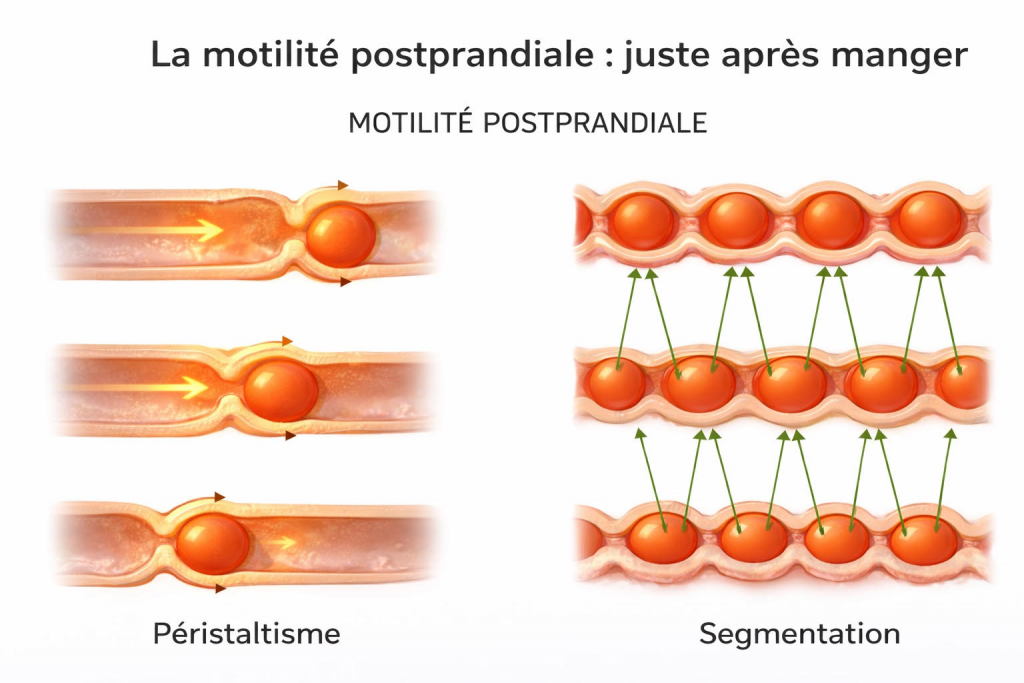
Le péristaltisme
Le péristaltisme correspond à une succession de contractions musculaires coordonnées qui permettent de faire avancer le contenu digestif le long de l’intestin.
Concrètement, après le passage des aliments dans l’estomac, ceux-ci sont transformés en une bouillie semi-liquide. Le péristaltisme permet alors d’acheminer progressivement ce contenu d’un point à un autre du tube digestif, assurant ainsi sa progression continue.
Son rôle principal est le transport.
La segmentation
La segmentation, quant à elle, ne vise pas à faire avancer le contenu digestif, mais à le mélanger (les brasser).
Ces mouvements alternent des contractions locales qui brassent les aliments à l’intérieur de l’intestin. Ce brassage favorise :
- La séparation fine des aliments,
- Leur mise en contact prolongée avec la muqueuse intestinale,
- Une absorption optimale des nutriments.
2. La motilité interprandiale (pendant les périodes de jeûne)
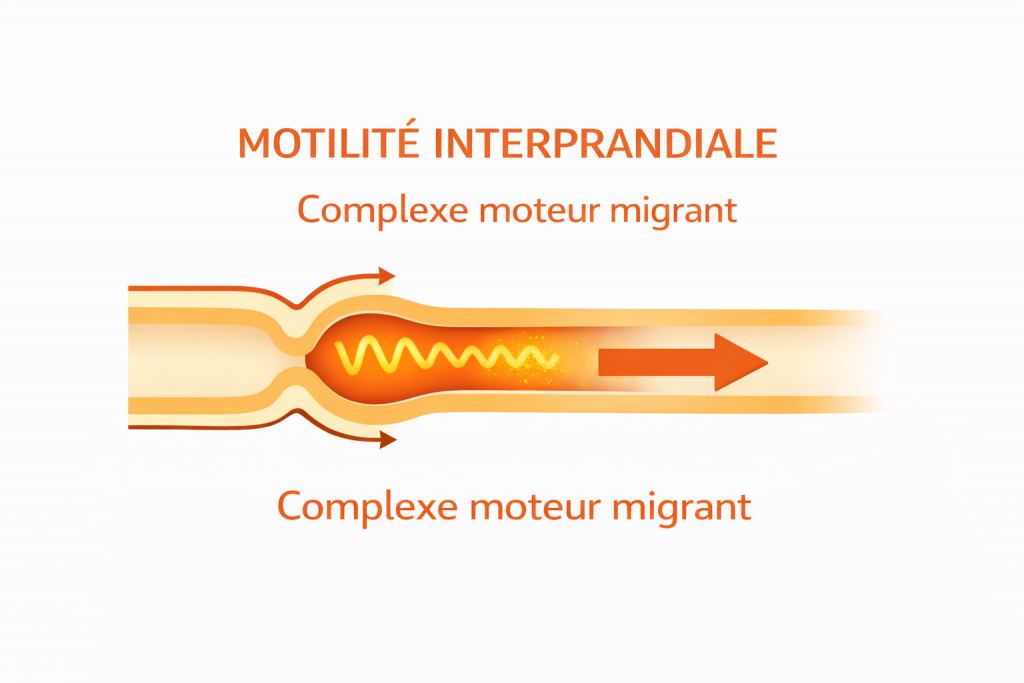
Le complexe moteur migrant (CMM)
Le complexe moteur migrant (CMM) est un cycle de contractions motrices rythmiques et coordonnées qui se produit dans le tube digestif en période de jeûne, principalement au niveau de l’estomac et de l’intestin grêle.
Son rôle physiologique est essentiel :
- Il permet le nettoyage mécanique de l’intestin grêle,
- Il favorise l’évacuation des résidus alimentaires, des sécrétions digestives et des bactéries vers le côlon,
- Il participe ainsi au maintien d’un équilibre microbiologique intestinal.
- Il augmente la production des enzymes digestives :
1. Diminution du PH acide de l’estomac
2. Augmentation de la production des acides biliaires et des sucs pancréatiques
Le CMM est un phénomène cyclique, survenant environ toutes les 1h30 à 3 heures en dehors des repas, et il est interrompu dès la prise alimentaire. Son fonctionnement dépend étroitement du système nerveux entérique, de l’intégrité de la muqueuse intestinale et de signaux neuro-hormonaux, notamment la motiline.
Une altération du CMM, même transitoire, peut compromettre ce mécanisme de “balayage intestinal” et favoriser la stagnation du contenu digestif dans l’intestin grêle.
Anatomie et physiologie du complexe moteur migrant (CMM)
Le complexe moteur migrant repose sur une organisation anatomique spécifique de la paroi intestinale, en particulier au niveau de la musculeuse, constituée de couches musculaires lisses circulaire et longitudinale. C’est dans cette région que se situent les éléments essentiels à la génération et à la propagation des contractions caractéristiques du CMM.
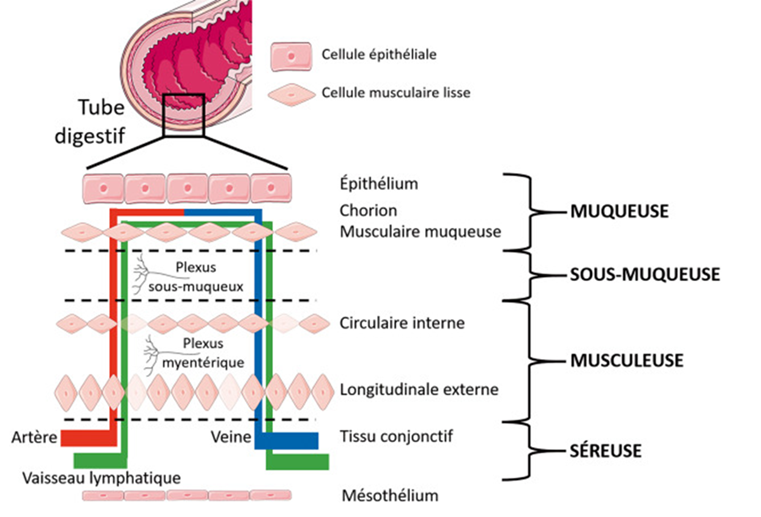
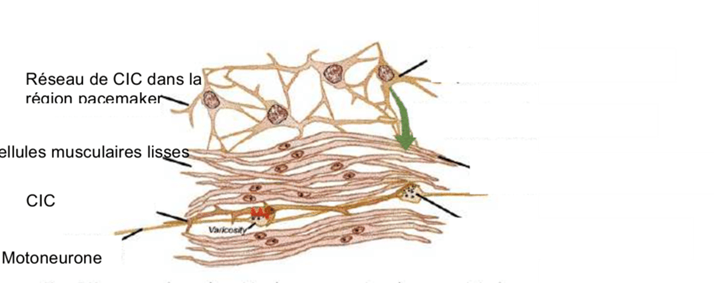
Au sein de la musculeuse, et plus précisément à l’interface entre les couches musculaires, au niveau du plexus myentérique, se trouve un réseau de cellules interstitielles de Cajal. Ces cellules constituent le pacemaker intestinal. À l’image du pacemaker cardiaque, elles sont capables de générer spontanément un rythme électrique de base, qui détermine la fréquence et l’organisation des contractions musculaires impliquées dans le CMM. Ce pacemaker est intrinsèque à l’intestin : il ne dépend pas du système nerveux cérébral pour fonctionner, mais son activité peut être modulée par le système nerveux entérique et le système nerveux autonome.
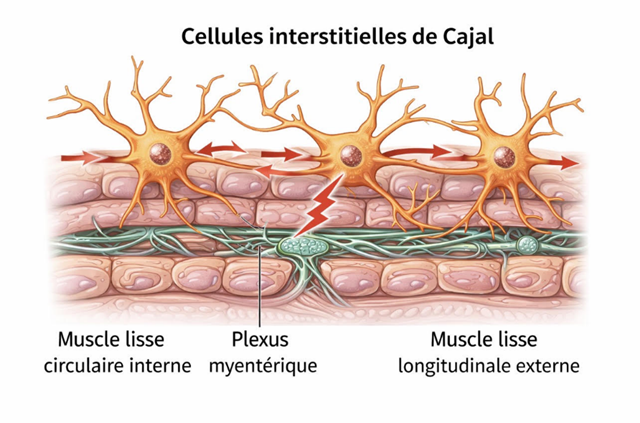
La physiologie du CMM ne repose pas uniquement sur la génération du signal rythmique, mais également sur sa propagation efficace le long du tube digestif. Cette propagation nécessite un couplage mécanique et fonctionnel entre les cellules musculaires lisses. À ce niveau intervient la vinculine, une protéine d’ancrage du cytosquelette, impliquée dans la liaison entre les filaments d’actine et la membrane cellulaire.
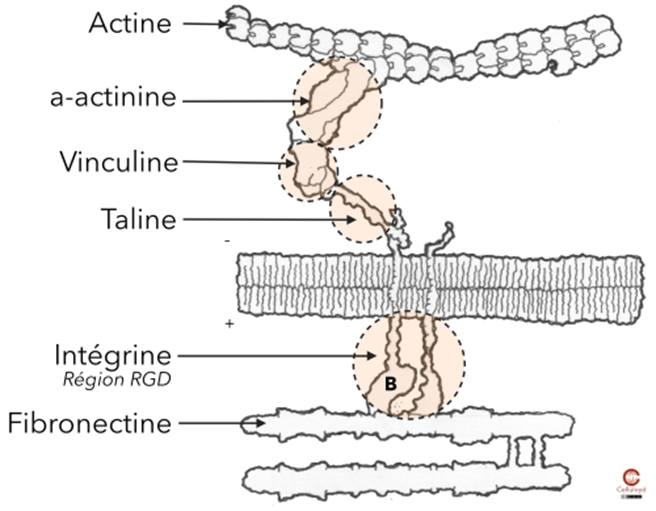
La vinculine
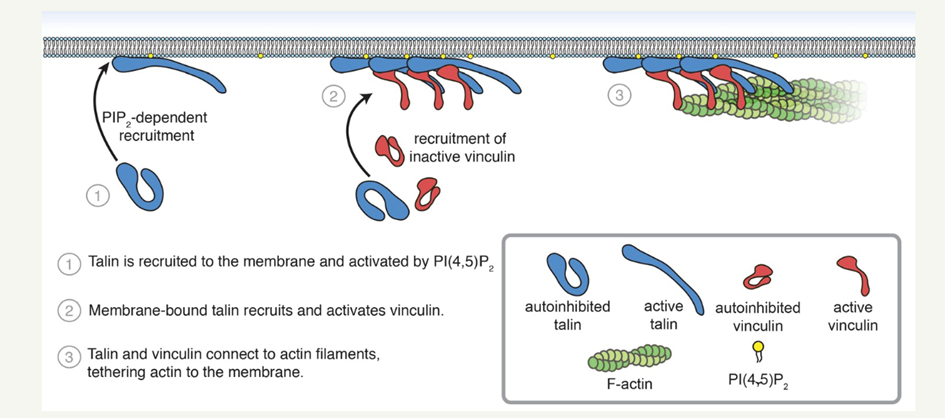
La vinculine est une protéine d’ancrage du cytosquelette localisée principalement au niveau des adhérences focales, structures spécialisées qui relient les filaments d’actine intracellulaires aux intégrines membranaires, elles-mêmes connectées à la matrice extracellulaire. Lorsque les cellules musculaires lisses se contractent, les forces générées par l’actomyosine sont transmises vers la membrane grâce à un complexe multiprotéique associant intégrines, taline et vinculine
Sous l’effet de la tension mécanique, la vinculine s’active et se lie à la taline ainsi qu’aux filaments d’actine. Elle renforce l’ancrage du cytosquelette à la membrane et stabilise les adhérences focales. Ce couplage permet une transmission efficace des forces mécaniques entre les cellules musculaires lisses, assurant la continuité de la contraction des couches musculaires circulaire et longitudinale.
Dans le tube digestif, cette fonction prend une importance particulière : la propagation des ondes lentes générées par les cellules interstitielles de Cajal doit s’accompagner d’une réponse mécanique homogène des cellules musculaires lisses. La vinculine contribue ainsi à transformer un signal électrique local en une réponse contractile coordonnée à l’échelle du tissu.
Ainsi, la physiologie de la contraction musculaire digestive repose non seulement sur des mécanismes électrophysiologiques et neuronaux, mais également sur une intégration mécano-cellulaire fine, dans laquelle la vinculine apparaît comme un élément clé du couplage entre signal, force et mouvement.
Intoxication alimentaire et vinculine
Certaines infections digestives bactériennes, notamment causées par Escherichia coli, Shigella, Salmonella ou Campylobacter jejuni, sont capables de produire une toxine appelée cytolethal distending toxin B (CDT-B). À la suite d’une gastro-entérite infectieuse, l’organisme met en place une réponse immunitaire dirigée contre cette toxine, avec la production d’anticorps anti-CDT-B.
Chez certaines personnes, ce mécanisme de défense devient délétère en raison d’un mimétisme moléculaire. Les anticorps anti-CDT-B reconnaissent par erreur une protéine de l’hôte présentant des similarités structurales : la vinculine. Il en résulte la production d’auto-anticorps anti-vinculine.
Or, comme on l’a dit précédemment, la vinculine joue un rôle fondamental dans la physiologie digestive. En se liant à la taline et aux filaments d’actine, elle permet la transmission et la coordination des forces mécaniques entre les cellules musculaires lisses. Elle participe ainsi au bon fonctionnement du complexe moteur migrant (CMM), indispensable au nettoyage du grêle entre les repas.
Lorsque la vinculine est altérée par ces auto-anticorps, elle ne peut plus assurer correctement son rôle d’ancrage et de transmission mécanique. Le couplage entre les cellules musculaires lisses devient moins efficace, ce qui perturbe la propagation des ondes contractiles. Le complexe moteur migrant est alors ralenti, affaibli ou désorganisé.
Cette altération du CMM favorise la stase du contenu intestinal, créant un terrain propice à la prolifération bactérienne dans l’intestin grêle. Ce mécanisme constitue aujourd’hui l’un des modèles physiopathologiques majeurs expliquant le développement du SIBO, en particulier dans ses formes post-infectieuses.
Ainsi, le SIBO ne résulte pas uniquement d’un déséquilibre bactérien, mais peut être la conséquence d’une atteinte immuno-mécanique du système moteur intestinal, impliquant la vinculine, les cellules interstitielles de Cajal et le muscle lisse digestif.
Conséquences d’un CMM altérée
Lorsque ce couplage est altéré, comme décrit précédemment, notamment en lien avec une atteinte de la vinculine par des auto-anticorps post-infectieux, la motricité intestinale devient désorganisée. Les cellules musculaires lisses restent capables de se contracter, mais la transmission des forces mécaniques est incomplète et mal synchronisée.
Le complexe moteur migrant perd alors sa continuité : les ondes de contraction sont fragmentées, plus courtes ou moins efficaces. Le nettoyage intestinal devient insuffisant, entraînant une stagnation progressive du contenu intestinal. Cette stase favorise l’accumulation bactérienne et participe au développement des symptômes digestifs caractéristiques du SIBO, tels que les ballonnements et les douleurs abdominales.
Ainsi, comme discuté précédemment, il ne s’agit pas d’une disparition de la contraction musculaire, mais d’une altération de sa coordination et de sa propagation, conséquence directe d’un défaut de transmission mécano-cellulaire.
SIBO à hydrogéne et symptômes
Après une intoxication alimentaire, il arrive fréquemment que les symptômes persistent et que le gastro-entérologue évoque un trouble « fonctionnel » de type SII-D. Dans cette configuration post-infectieuse, parmi les trois proliférations possibles (SIBO à hydrogène, SIBO à sulfure d’hydrogène, IMO/méthanogènes), le profil le plus cohérent est celui du SIBO à hydrogène : fermentation rapide, production de gaz et transit plutôt accéléré.
Symptômes digestifs (les plus fréquents, et souvent très évocateurs)
- Ballonnements précoces (parfois dès le début du repas)
- Ventre visiblement distendu / sensation de “gonflement”
- Douleurs abdominales (diffuses, crampes, spasmes)
- Flatulences et borborygmes
- Selles molles / diarrhées, parfois urgences
- Inconfort post-prandial : sensation de trop-plein, gêne digestive rapide
- Intolérance alimentaire fluctuante, en particulier aux aliments très fermentescibles (fruits, certaines fibres, légumineuses, etc.)
Symptômes associés (souvent rapportés)
- Fatigue (souvent post-prandiale)
- Brouillard mental, difficultés de concentration
- Sensation de malaise après les repas (profil neurovégétatif chez certains)
- Variabilité jour après jour, avec des poussées selon le stress et l’alimentation
Pourquoi les antibiotiques améliorent souvent (au moins temporairement)
Un point important, souvent rapporté, est que les antibiotiques diminuent fréquemment les symptômes. La raison est simple : en réduisant transitoirement la charge bactérienne dans l’intestin grêle, ils réduisent les fermentations et donc la production de gaz. Cela peut entraîner une amélioration nette du ventre gonflé, des douleurs et des selles. (Cette amélioration n’est pas toujours durable si la cause sous-jacente — notamment la motricité — n’est pas corrigée.)
Pourquoi les probiotiques peuvent aggraver
À l’inverse, les probiotiques peuvent aggraver chez certains patients : l’idée n’est pas qu’ils soient “mauvais”, mais que, dans un intestin déjà en surcharge, ajouter des bactéries (même “bénéfiques”) peut augmenter les fermentations, la production de gaz et donc les ballonnements et douleurs. C’est une des raisons pour lesquelles certains patients décrivent une aggravation nette dès l’introduction de probiotiques, surtout au début.
Les tests diagnostiques du SIBO et de l’IMO
Plusieurs méthodes permettent aujourd’hui d’orienter ou de confirmer un diagnostic de SIBO ou d’IMO. Aucune n’est parfaite : chacune présente des avantages, des limites et un champ d’application précis. L’interprétation doit toujours être contextualisée aux symptômes et à l’histoire clinique.
1. Le test respiratoire à l’hydrogène et au méthane
Le test respiratoire est actuellement l’outil le plus utilisé en pratique clinique, car il est simple, non invasif et peu coûteux.
Principe :
Après ingestion d’un substrat (glucose ou lactulose), on mesure dans l’air expiré la production de gaz issus de la fermentation bactérienne :
- hydrogène → suggère un SIBO à hydrogène
- méthane → suggère un IMO (prolifération de méthanogènes)
Ces gaz, produits dans l’intestin, passent dans le sang puis sont éliminés par les poumons, ce qui permet une mesure indirecte de l’activité microbienne intestinale.
Points clés :
- Utile pour dépister SIBO et IMO
- Résultat influencé par la préparation au test (alimentation, transit, médicaments)
- Sensibilité et spécificité variables selon le protocole
- Ne permet pas, à lui seul, d’identifier l’origine du trouble moteur
Il reste néanmoins l’examen de première intention dans la majorité des cas.
2. L’aspiration du liquide de l’intestin grêle par endoscopie
Cette méthode consiste à prélever directement le contenu de l’intestin grêle (duodénum ou jéjunum) afin de quantifier les bactéries présentes.
Principe :
- Endoscopie digestive haute
- Aspiration de quelques millilitres de liquide
- Analyse microbiologique en laboratoire
Un excès bactérien au-delà d’un seuil défini permet de poser un diagnostic de SIBO.
Limites majeures :
- Examen invasif
- Coût élevé
- Accès limité
- Représente une zone restreinte de l’intestin grêle
Bien que considérée comme une référence théorique, cette technique est peu utilisée en pratique courante, notamment en France.
3. Les tests sanguins (anticorps anti-vinculine et anti-CDT-B)
Ces analyses visent à identifier un mécanisme post-infectieux, plutôt qu’une prolifération bactérienne directe.
Principe :
- Recherche d’anticorps dirigés contre :
- la toxine bactérienne CDT-B
- la vinculine, protéine clé du complexe moteur migrant
- Mise en évidence d’un processus auto-immun post-infectieux
Ces tests permettent d’identifier les patients chez qui une intoxication alimentaire a entraîné une atteinte durable de la motricité intestinale.
Points importants :
- Spécifiques des SIBO post-infectieux
- Ne détectent pas les autres formes de SIBO ou d’IMO
- Actuellement disponibles essentiellement aux États-Unis
- Encore en cours de validation clinique élargie
Solutions et perspectives
Le but de cet article était de vous éclairer sur la cause principale du syndrome de l’intestin irritable (SII) post-infectieux ainsi que du SIBO à hydrogène.
Bien que je vous propose ici quelques pistes de réflexion, la solution la plus efficace reste de consulter un professionnel de santé afin de bénéficier d’un accompagnement personnalisé. Je vous conseille vivement de vous tourner vers un gastro-entérologue, un diététicien ou un naturopathe spécialisé pour établir un protocole adapté à votre situation.
Approche Intégrative du SIBO Hydrogène et du SII Post-Infectieux
I. L’Impératif du Diagnostic
Avant d’envisager toute cure d’antimicrobiens, aussi naturels soient-ils, un diagnostic médical précis (test respiratoire au glucose ou lactulose) est indispensable. On ne traite pas un SIBO supposé : les plantes puissantes comme la berbérine ou l’origan ne doivent être utilisées que si la présence de bactéries dans l’intestin grêle est confirmée, afin de ne pas léser inutilement le microbiote colique.
1. Les antimicrobiens (Diagnostic et suivi médical impératifs auprès d’un professionnel de santé)
L’intervention sur la population bactérienne doit être ciblée. Les dosages suivants sont ceux couramment observés en pratique clinique :
- Berbérine : 500 mg, 3 fois par jour (soit 1500 mg/j).
- Huile essentielle d’Origan (capsules gastro-résistantes) : 150 à 200 mg, 2 x fois par jour.
- Neem (Margousier) : 300 à 500 mg, 3 fois par jour.
- Cannelle (Cinnamomum cassia) : 500 mg, 2 fois par jour pour son action antifongique et antibactérienne complémentaire.
2. Relance de la motilité (Prokinétiques naturels)
Le soutien du Complexe Moteur Migrant (CMM) est le pilier de la prévention des récidives.
- Gingembre (extrait standardisé) : Jusqu’à 2000 mg/jour .
- Artichaut (extrait de feuilles) : 200 à 400 mg/jour. La synergie Gingembre/Artichaut est privilégiée le soir au coucher.
- 5-HTP : 100 mg à 200 mg au coucher pour soutenir la sérotonine endogène, moteur du péristaltisme.
3. Gestion symptomatique et Adsorption
Ces outils sont utilisés ponctuellement pour gérer l’inconfort lié aux gaz et aux toxines (LPS).
- Charbon actif : 500 mg à 1g, à prendre au moins 2 heures après toute autre médication (capacité d’adsorption élevée).
- Argile verte (ultra-ventilée) :
- Menthe poivrée & Carvi : 1goutte de chaque dans un peu d’huile de coco 3 x par jour
4. Réparation de la barrière épithéliale et Inflammation
- Zinc Carnosine : 75 mg, 1 à 2 fois par jour. Forme spécifique pour la cicatrisation gastrique et duodénale.
- L-Citrulline : 5 à 10 g, 1 à 2 x fois par jour pour optimiser la perméabilité inestinale
- Butyrate (Acide butyrique) : 500 mg à 1g par jour. Acide gras à chaîne courte essentiel à l’homéostasie du côlon et à la réparation épithéliale.
- Curcumine (haute biodisponibilité) : 500 mg, 2 fois par jour pour moduler l’inflammation de bas grade.
5. Soutien Probiotique ciblé (Souches non-fermentescibles)
L’utilisation de probiotiques en cas de SIBO doit se limiter à des souches ne risquant pas d’augmenter la charge bactérienne du grêle.
- Saccharomyces Boulardii : 250 à 500 mg, 2 fois par jour. Indispensable en post-infectieux pour réguler l’immunité intestinale.
- Bacillus Coagulans & Bacillus Subtilis : 1 à 2 milliards d’UFC par jour. Ces bactéries sporulées traversent le grêle sans y stagner.
6. Stratégies Nutritionnelles
- Le Régime Low-FODMAP (Approche Symptomatique)
C’est la stratégie de première intention pour réduire la pression gazeuse et les douleurs. L’objectif est de limiter les Glucides Fermentescibles à Chaîne Courte.
- Mécanisme : Ces sucres sont mal absorbés dans l’intestin grêle et arrivent intacts dans le côlon (ou sont fermentés trop tôt en cas de SIBO), provoquant un appel d’eau (diarrhée) et une production de gaz (ballonnements).
- Les familles exclues :
- Fructanes & GOS : Blé, seigle, ail, oignons, poireaux, artichauts, légumineuses.
- Lactose : Produits laitiers classiques (vache, chèvre, brebis).
- Fructose en excès : Pommes, poires, miel, sirop de maïs.
- Polyols : Édulcorants (sorbitol, xylitol), champignons, abricots, chou-fleur.
- Application : Phase d’éviction de 4 à 6 semaines, suivie d’une phase de réintroduction méthodique par famille pour identifier les seuils de tolérance personnels.
- Le Régime Bi-Phasique (Sibo Bi-Phasic Diet)
Développé spécifiquement pour le SIBO par le Dr Nirala Jacobi, il combine les principes du Low-FODMAP et du régime SCD pour optimiser l’efficacité des antimicrobiens.
- Phase 1 : Réduction (2 à 4 semaines)
- Objectif : Réduire drastiquement la fermentation pour affamer les bactéries avant l’attaque.
- Aliments autorisés : Viandes, poissons, œufs, graisses saines (huile d’olive, ghee), et une liste très restreinte de légumes (carottes, courgettes pelées, haricots verts en petite quantité). Toutes les céréales, les féculents et les sucres sont exclus.
- Phase 2 : Éradication (4 à 6 semaines)
- Objectif : Accompagner la prise des antimicrobiens.
- Aliments autorisés : On réintroduit une petite quantité de riz basmati ou de quinoa. L’idée est de « réveiller » les bactéries restantes par une légère fermentation pour les rendre plus vulnérables aux traitements antimicrobiens.
3. Le Régime sans Glucides Spécifiques (SCD – Specific Carbohydrate Diet)
C’est le régime le plus structurel, souvent utilisé en cas de dommages profonds à la muqueuse (ulcères, maladie de Crohn, hyperperméabilité sévère).
- Mécanisme : Il repose sur l’exclusion de tous les disaccharides (sucres doubles) et polysaccharides (amidons). Le corps ne doit ingérer que des monosaccharides (sucres simples), qui sont absorbés instantanément sans effort enzymatique complexe.
- Les exclusions majeures :
- Toutes les céréales (même le riz et le quinoa).
- Tous les féculents (pommes de terre, patates douces, maïs).
- Tous les sucres raffinés et le lactose.
- Les autorisations : Fruits frais, légumes (bien cuits), miel, viandes, poissons, œufs, noix (si tolérées) et certains fromages affinés plus de 24h (sans lactose).
- Bénéfice : En supprimant les amidons, on stoppe la source de nourriture principale des bactéries et on permet aux villosités intestinales (aidées par la Citrulline et le Zinc Carnosine) de se régénérer sans l’agression des toxines de fermentation.
On arrive à la fin de cet article. Les informations de ces solutions sont générales et ne remplacent pas un accompagnement personnalisé. Si vous souhaitez adapter ces conseils à votre situation et être accompagné(e) dans votre démarche, je vous invite à prendre rendez-vous en cliquant sur le lien https://www.crenolibre.fr/prendre-rdv/10848_cedric-schmidt-naturopathe-a-lyon
